Haruldase haigusega mees saab novaatorlikku geeniravi (1)
44-aastane Brian Madeux põeb Hunteri sündroomi, mida nimetatakse ka II tüüpi mukopolüsahharidoosiks. Haige keha ei tooda ensüümi, mis lagundaks glükosaminoglükaane. Need polüsahhariidid hakkavad kehasse kogunema ning organeid kahjustama. See tekitab hingamisraskusi, pidevaid põletikke, kahjustab aju, samuti ei saa haiged kõndida ning surevad üsna noorelt.
Haruldast pärilikku tõbe põevad peamiselt mehed. Põhjus on selles, et haigust põhjustav geen asub X-kromosoomis. Naistel on kaks X-kromosoomi ja nad põevad Hunteri sündroomi vaid siis, kui mõlemas kromosoomis on vigane geenikoopia. Ühe nii-öelda katkise geeniga naised on vaid haiguse kandjad. Meestel on ainult üks X-kromosoom ja kui seal on sündroomi tekitav geenivariant, tekibki haigusseisund.
Hunteri sündroomiga inimesi tuleb ilmale keskmiselt üks iga 100 000 kuni 170 000 sünni kohta. Siiani pole haiguse vastu head ravi. Näiteks kasutatakse teraapiat, kus igal nädalal tilgutatakse veeni kaudu kehasse puuduva ensüümi koopiat, mis hakkab kehasse kogunevaid aineid lagundama. Kui eksperiment õnnestub, on käeulatuses võimalus panna rakud ise vajalikku ensüümi tootma.
Keemilised käärid
Praegu kasutavad molekulaarbioloogid vigaste geenide asendamisel tervetega enamasti CRISPR-meetodit. See bakteritelt laenatud DNA kleepimise ja lõikamise süsteem on muutunud menukaks viimase 3-4 aasta jooksul ning lubab geenidega täpsemalt manipuleerida.
Sangamo teadlased üritavad Madeux' DNAsse terveid geenikoopiad sisestada teist tüüpi molekulaarsete kääridega, mida tuntakse tsinksõrme nukleaasidena (zinc finger nuclease ehk ZFN). Loodetakse, et geenid jõuavad maksarakkudesse ja hakkavad seal vajalikku ensüümi tootma.
Loomulikult on iga eksperimentaalteraapia seotud võimalike kõrvalmõjudega. Ajakiri Science tõi välja kaks peamist ohtu. Nimelt kasutatakse geenivektorina viirust, mida peetakse küll ohutuks, kuid see võib mõnel patsiendil siiski esile kutsuda immuunvastuse, mida peab põletikuvastaste ravimitega ohjes hoidma. Samuti on olemas oht, et ZFN-käärid võivad DNAd lõigata valest kohast ja ellu äratada mõne vähitekkega seotud geeni.
Väidetavalt hakatakse uut ravi saavatelt haigetelt edaspidi võtma maksa koeproove ja uuritakse neis toimunud DNA-muutusi. Skeptikud kardavad siiski, et kuna mõned kasvajad arenevad väga aeglaselt, ei pruugita vähiteket piisavalt kiiresti avastada. Optimistide arvates on Sangamo Therapeutics saanud koekultuuris ja loomkatsetes piisavalt häid tulemusi ning uue raviviisi inimestel katsetamine on tänuväärne samm.
26 operatsiooni
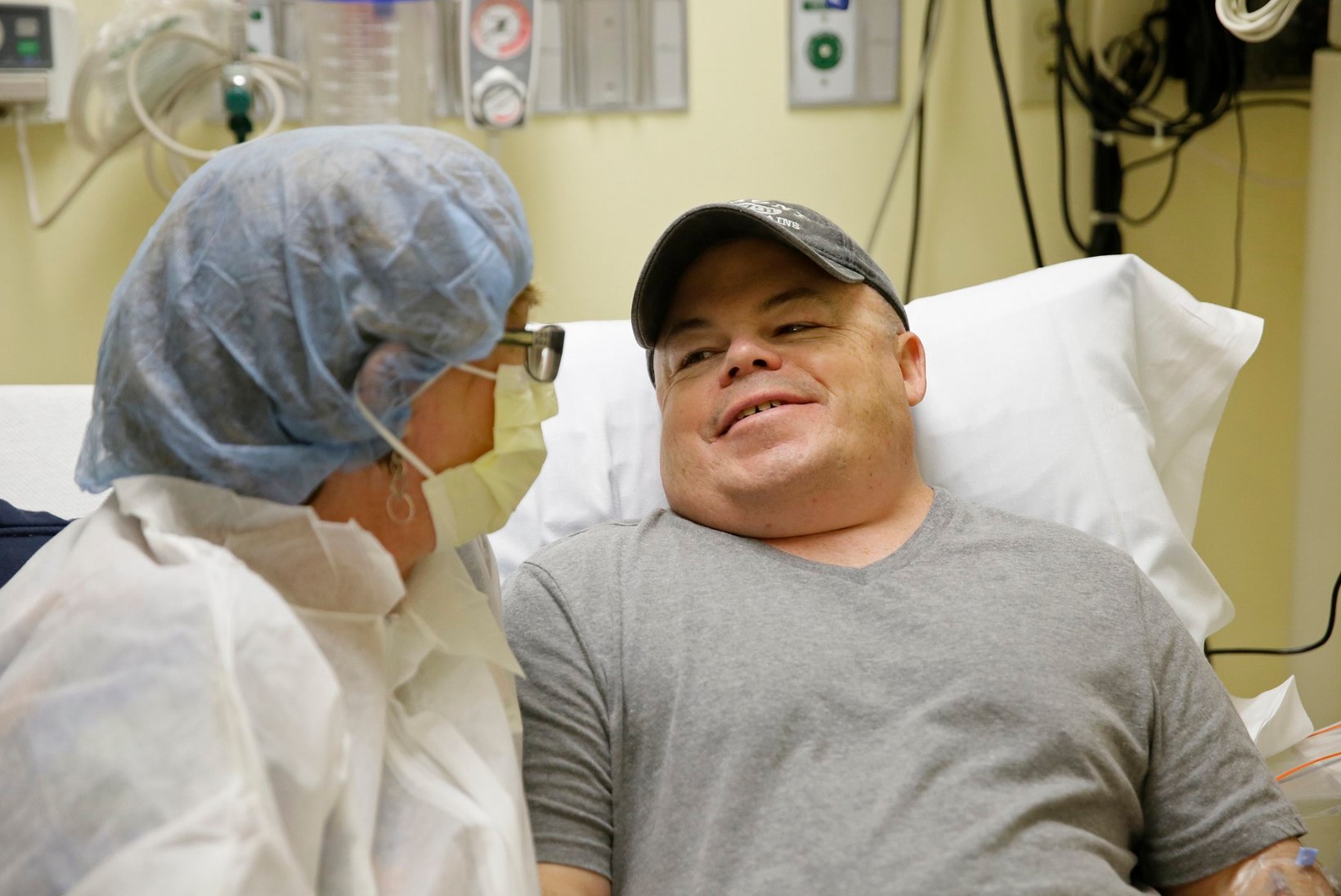
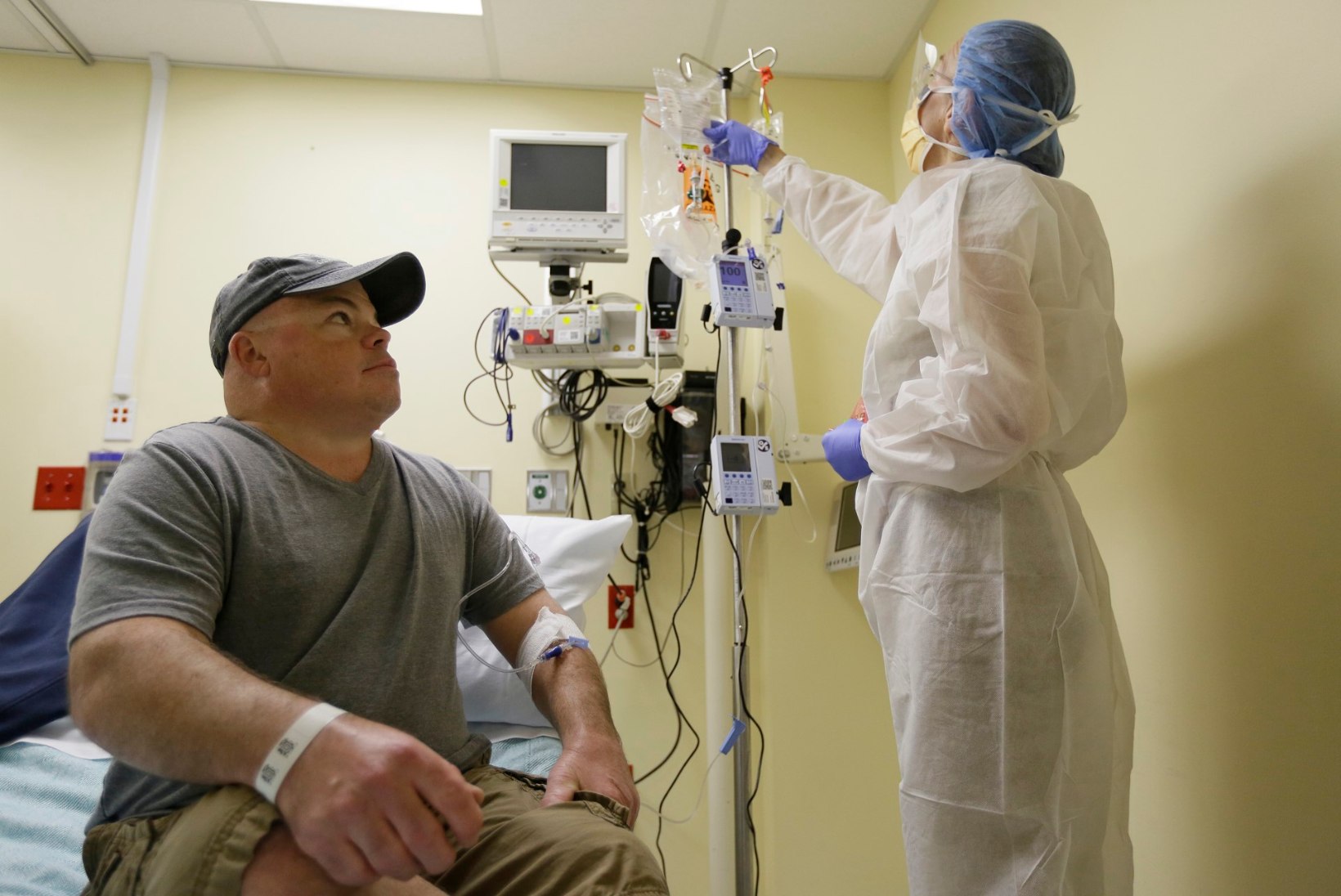
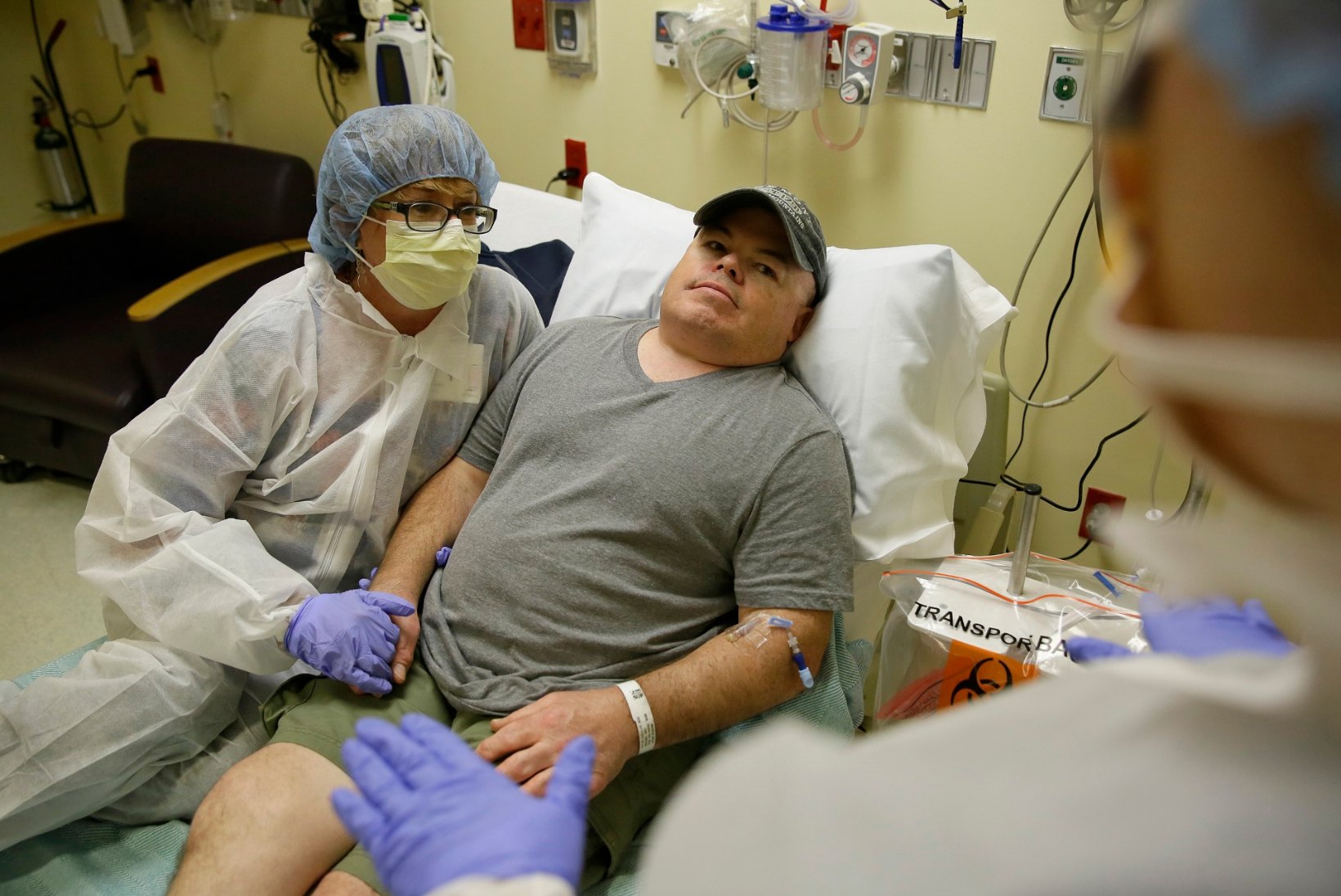
Ka Madeux kinnitas, et tal on suured lootused. Intervjuus ajalehele Guardian ütles mees, et ta on pidanud läbi tegema 26 operatsiooni: lõigatud on songa, praavitatud haiget selga, leevendatud kõrva- ja silmahädasid. Läinud aastal oleks bronhiit ja kopsupõletik ta peaaegu hauda viinud. Nüüd loodab Madeux, et geeniteraapia säästab talle edaspidi eelkõige aega. Siiani on mees igal nädalal pidanud haiglas käima, kus talle vajalikku ensüümi verre tilgutatakse.
Sangamo teadlased plaanivad uut geeniravi katsetada kokku kuni 30 täiskasvanul, et veenduda selle täielikus ohutuses. Tulevikus aga loodetakse ravida juba pisikesi lapsi, kelle keha ensüümipuudulikkus veel kahjustada pole jõudnud. Ka Madeux rõhutas, et ta loodab katsest tulu eelkõige pisikestele Hunteri sündroomi põdejatele, kelle elundid on veel terved.
Kommentaarid